湖南大学宋国胜教授实验室近年来工作概览
宋国胜教授简介

宋国胜,湖南大学-化学化工学院,教授。2014年博士毕业于东华大学(导师:胡俊青)。2014 - 2018年在苏州大学(导师:刘庄)和美国斯坦福大学-医学院(导师:Jianghong Rao)从事博士后研究。2018年入职湖南大学(教授),加入化学生物传感与计量学国家重点实验室。宋国胜的研究工作主要针对活体成像中存在的灵敏度低和信号干扰因素多等难题,发展了高信号强度、可激活和比率型的光学或磁性纳米探针,通过MPI、MRI、化学发光、光声、长余辉等成像,实现对肿瘤和心血管疾病的全身和高灵敏成像以及疗效监测。发表第一或通讯作者论文30余篇,包括Nat. Biomed. Eng.、Chem、JACS、Angew. Chem.、Adv. Mater.、Nano Lett.、ACS Nano、Adv. Funct. Mater.、Chem. Soc. Rev.、Coord. Chem. Rev.、Anal. Chem.、Chem. Sci.、Biomaterials、Small、Sci. China Chem.、CCS Chem.等权威期刊。其中“IF> 10”的期刊20余篇;论文总引用>6000次;SCI “H-index”为42;入选教育部“长江学者”青年学者、湖南省“芙蓉学者”特聘教授。

宋国胜教授实验室合照
下面本文将选取三个方面具有代表性的文章来简要介绍宋国胜教授实验室近年来所取得的成绩。
(一)化学发光和化动力治疗
化学发光(CL)成像依靠化学反应释放的能量,由于没有激光激发,在无干扰的背景噪声下具有广阔的应用前景。然而,CL体系在体内清除困难、发光弱、发射波长短等缺点,阻碍了大多数CL系统在体内成像方面的应用。化学动力学疗法(CDT)利用纳米催化剂通过Fenton-like催化反应,将内源性双氧水催化生成具有细胞杀伤性的活性氧(ROS)。然而,肿瘤微环境的微酸性(pH 6.5-6.9)不能满足高效的芬顿反应发生的酸性条件(pH 3.0-5.0),以及不可避免的“脱靶”毒性。在此基础上,宋国胜教授致力于开发新型的化学发光体系并用于化动力治疗监测以及开发新型CDT策略从而实现高效、特异性的肿瘤治疗。
(1)CL成像引导CDT纳米平台
该实验室设计并合成了一种用于CL成像引导CDT的有机半导体聚合物纳米平台(图1)。他们将葡萄糖氧化酶、化学发光底物过氧草酸酯、近红外发射染料、催化剂血红素整合到他们的纳米平台上,在双氧水/葡萄糖存在时能显着地增强CL成像和CDT(Nano Lett., 2020, 20, 176-183)。

图1. 纳米平台的合成及化学发光机理图。
该纳米平台可以克服CL发光弱、闪光型发射、波长短的主要缺点,进一步促进了CL成像在体内的应用。重要的是,他们的纳米平台能够建立体外良好的CL成像强度与ROS产率之间的相关性,进一步建立了活体CL成像强度与CDT后肿瘤抑制率之间的良好相关性(图2)。
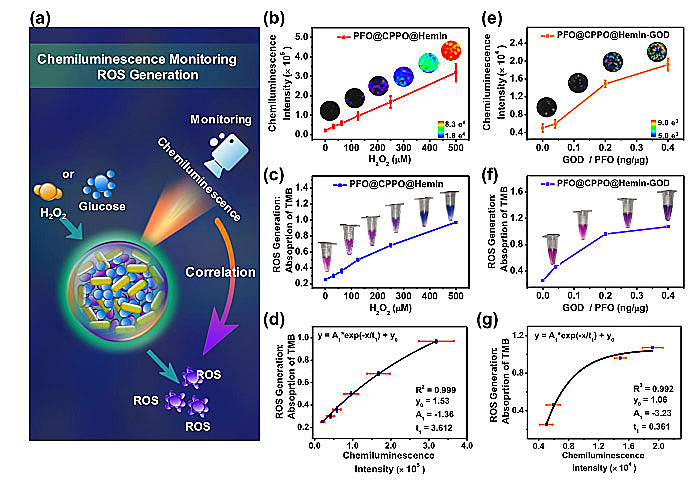
图2. (a)化学发光监测ROS生成机制示意图。(b-g) 化学发光强度与ROS产量的相关性。
(2)锰-噻吩新型化学发光体系
该实验室设计并构建了一种新型的基于锰-噻吩的化学发光(CL)成像和化学动力学治疗(CDT)体系,并能够利用CL和荧光(FL)比率型成像引导CDT实现肿瘤治疗的实时原位监控(图3)。
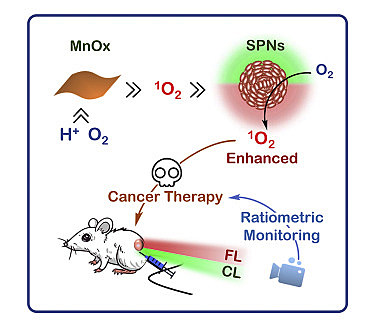
图3. 新型化学发光体系引导化学动力疗法示意图。
该研究提出了基于锰-噻吩的化学发光体系的反应机理(图4),锰氧化物在酸性条件下释放单线态氧(1O2);1O2可以通过π2-π2环加成将聚合物单元中的噻吩氧化,从而形成噻吩-二氧杂环中间体,该中间体能自然降解并产生化学能;所产生的化学能通过CIEEL过程转移到未氧化的半导体聚合物中,形成激发态的半导体聚合物。被激发的半导体聚合物能够同时产生CL和大量的1O2。
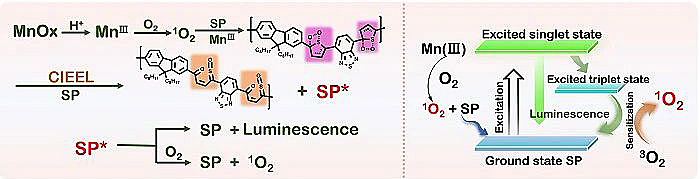
图4. 基于锰-噻吩的化学发光体系的反应机理示意图。
此外,由锰氧化物与半导体聚合物构成的纳米体系在酸激活下产生CL的同时也伴随着FL强度的降低。该体系能够在体外建立良好的比率型信号(CL/FL)与ROS产率之间的相关性(R2=0.992),并进一步建立活体CL/FL信号与CDT治疗后肿瘤抑制率之间的良好相关性(图5)。相关研究成果的研究论文发表在化学领域顶级期刊Chem(Chem, 2020, 6, 2314-2334)。
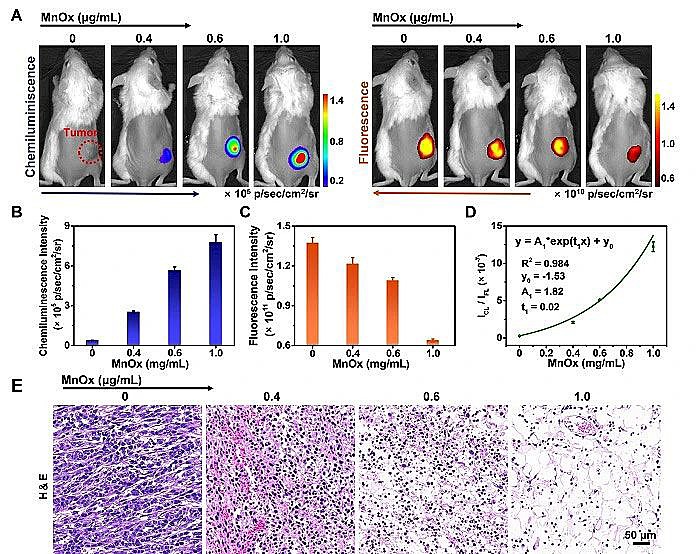
图5.(A-D)小鼠CL和FL图像及强度。(E)H&E染色各组肿瘤切片图像。
(3)新型化学动力学治疗策略
该实验室通过将核-壳结构FePt@FeOx纳米颗粒和pH响应的他莫昔芬(TAM)药物同时封装到聚合物聚苯乙烯-顺丁烯二酸酐(PSMA)中,并用聚乙二醇-氨基(PEG-NH2)对其进行改性,提出了一种新颖的策略来调节纳米催化剂用于癌症治疗的催化活性(图6)(Angew. Chem. Int. Ed., 2021, 60, 9562-9572)。
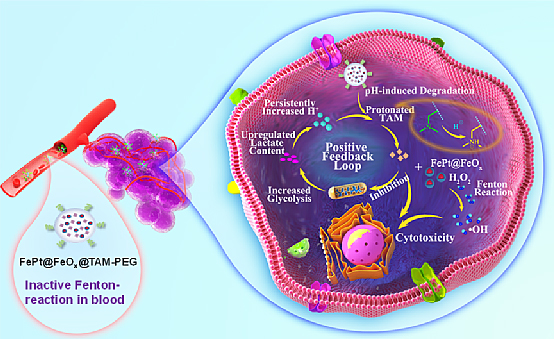
图6. 循环放大的纳米催化CDT治疗示意图。
该研究提出了高效且高特异性CDT的机制(图7),在肿瘤的微酸性条件下,由于TAM的pH响应,发生从疏水性到亲水性的TAM转变,FePt@FeOx@TAM-PEG被分解,释放出FePt@FeOx催化肿瘤内源性H2O2反应生成•OH;重要的是,释放的TAM作为线粒体复合物I的抑制剂能够增强糖酵解和乳酸含量,从而导致癌细胞内H+积累,从而克服了肿瘤微酸性的局限性;癌细胞酸化程度的升高可进一步促进FePt@FeOx@TAM-PEG的分解形成正反馈回路释放了更多FePt@FeOx纳米催化剂和TAM药物,并增强了它们在肿瘤中的催化活性,从而产生更高毒性的•OH诱导细胞凋亡。
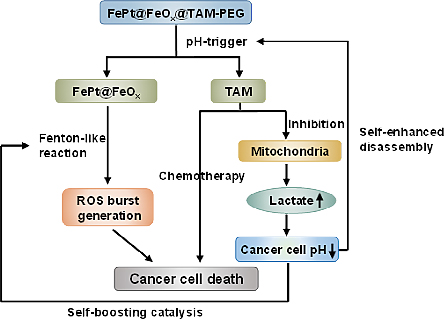
图7. 双通路自我扩增促进化学动力治疗的机制示意图。
(二)光声成像
光声成像是利用脉冲激光照射吸收光的组织或造影剂产生的光热膨胀产生的超声信号,是一种无创成像技术。与传统的荧光或生物发光成像技术相比,光声成像能够显著提高体内成像深度和空间分辨率。然而,大多数光声探头都受到单因素激活或单信号输出的影响,使得光声成像的特异性和准确降低。因此该实验室灵活构建基于两个或多个互不干扰的检测信号比值作为信号输出的比率型光声探针,来实现高特异性的光声成像。
(1)可激活的比率半导体纳米颗粒
该实验室通过将超氧阴离子响应的ORM和不敏感的OIM同时封装到两亲性聚合物DSPE-PEG中,开发了一种可激活的比率半导体纳米颗粒(RSPN),用于动脉粥样硬化合并肺炎斑块超氧阴离子(O2•-)的比率光声成像,从而评估易损性斑块的风险性。
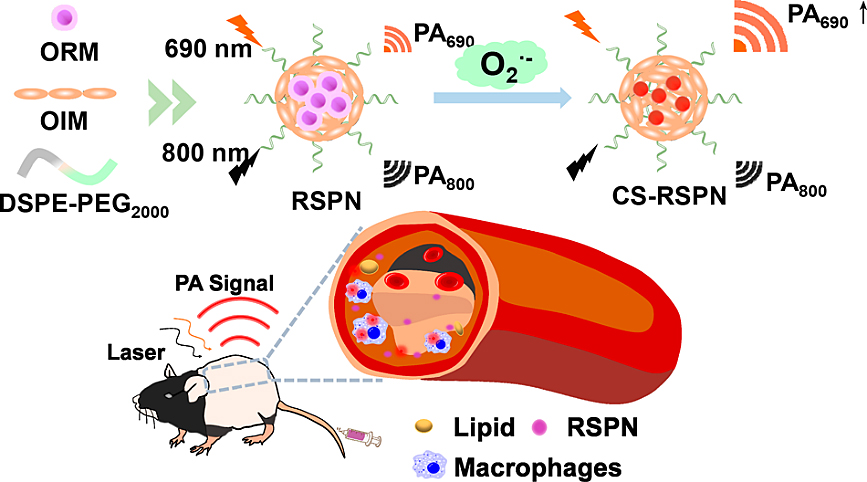
图8. RSPN合成过程及比率光声成像示意图。
该研究中ORM与斑块内超氧阴离子反应后实现690 nm光声信号的开启,性质稳定的OIM可以在800 nm处提供可靠的光声内参信号,因此,升高PA690/PA800的比率光声信号可以作为检测O2•-的指标。在肺炎合并的动脉粥样硬化小鼠中,主动脉区域显著升高的PA690/PA800信号可以评估超氧阴离子含量,从而实现主动脉斑块氧化应激水平的实时监控(Nano Lett., 2021, 21, 4484-4493)。
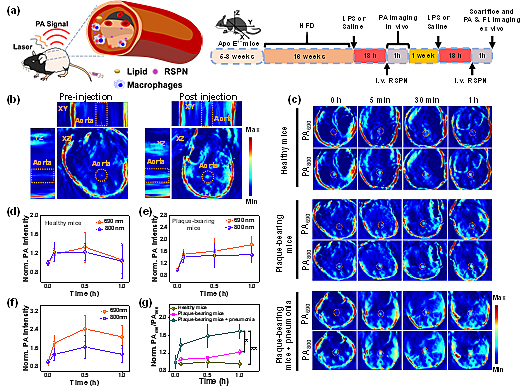
图9. 肺炎合并的动脉粥样硬化小鼠模型中的光声信号。
(2)“双钥匙-单锁”智能纳米探针
基于肿瘤微环境中较高水平的NO和低pH值的特性,团队设计合成了NO/酸共激活的(D-π-A-π-D)型响应分子,同时合成了另一种惰性分子作为内参,通过组装形成“双钥匙-单锁”智能纳米探针(图10)。只有在NO和酸的共激活下,纳米探针的光声、光热性能开启,通过输出比例光声、光热信号,用于高特异性的肿瘤成像和肿瘤光热治疗(J. Am. Chem. Soc., 2019, 141, 13572-13581)。
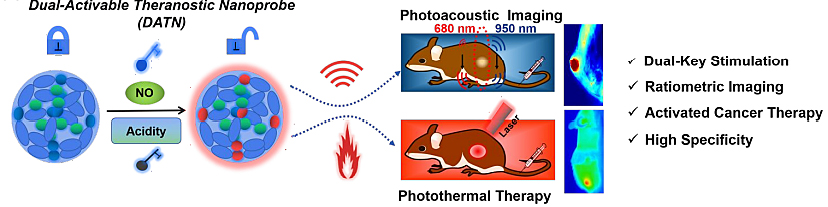
图10. 探针用于高特异性的肿瘤成像和光热治疗示意图。
(3)普鲁士蓝纳米探针
该实验室开发了一种基于普鲁士蓝(PB)的可激活纳米探针,它可以结合光声成像(PAI)和磁共振成像(MRI)对深部组织中的ONOO-进行成像。该研究首次发现ONOO-可以破坏PB的晶体结构,使得PB在710 nm处的强吸收大大减弱。因此,PB降低的光声成像信号可以作为检测ONOO-的指标。在此基础上,作者进一步设计并合成了一种以CuS为核心、PB为外壳的核壳CuS@PB纳米探针,用于产生比值光声信号从而实现快速准确地检测ONOO-(图11)(Anal. Chem., 2020, 92, 13452-13461)。
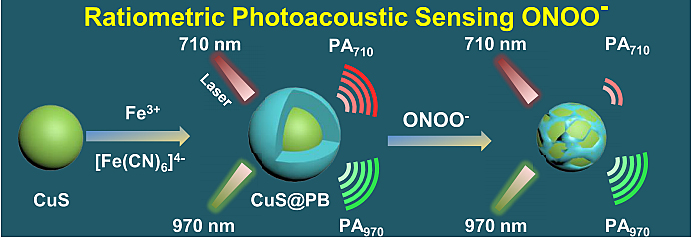
图11. CuS@PB纳米探针制备及检测ONOO-原理图。
(三)磁共振成像和磁性粒子成像
磁共振成像(MRI)通过检测磁对比的松弛信号,具有无限的组织穿透深度和高的空间分辨率,适合于术前检测深层恶性肿瘤。然而,无论是否与肿瘤生物标记物相互作用,大多数MR造影剂都是“始终开启”的信号。这可能导致低信号-背景比,使其难以突出感兴趣的生物现象。磁性粒子成像(MPI)与MRI不同是,MPI是通过直接探测磁性粒子在磁场中的响应性变化,实现对磁性粒子空间分布的直接成像。目前,MPI的关键瓶颈在于缺乏有效MPI造影剂。如果直接将MRI的造影剂用于MPI,通常会产生较弱的MPI信号或者无MPI信号。针对这些问题,宋国胜教授实验室致力于开发能够产生高度特异性反应的可激活MRI探针以及高效磁性粒子造影剂。
(1)可激活的光磁纳米平台
该实验室开发了第一个H2S激活的“一匙三锁”双金属纳米片(Gd/Cu-纳米片),该纳米片具有可激活的磁共振成像,荧光,光动力效应(图12)。他们将Gd掺杂的四羧基卟啉与铜离子通过水热微乳法形成Gd/Cu双金属纳米粒子。通过片层剥离,得到Gd/Cu-纳米片。通过结合MRI/荧光成像双模成像的互补优势,在H2S激活后,Gd/Cu-nanosheets可实现细胞和体内结肠癌的高特异性可视化(CCS Chem., 2020, 2, 2126-2142, DOI: 10.31635/ccschem.020.202000369)。
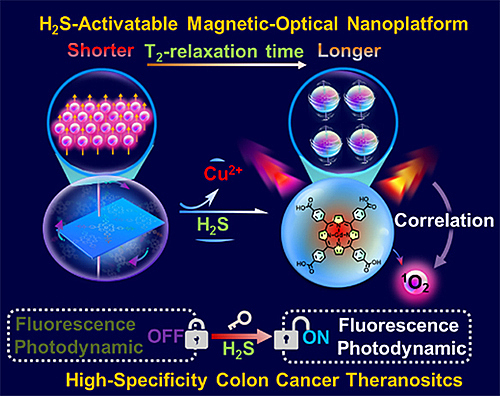
图12.光磁纳米平台示意图。
(2)高效磁性粒子成像造影剂
宋国胜教授与斯坦福大学Rao Jianghong教授合作,通过系统的研究,获得了影响MPI成像信号的作用规律和关键原理,开发了新型磁性粒子探针(FeCo合金粒子)。其FeCo合金粒子的MPI信号强度是商用造影剂的6-15倍。MPI直接探测磁性粒子在磁场中的响应性变化,相对于MRI检测水质子的弛豫率的信号来说,FeCo磁性粒子在MPI中产生的磁化率是水质子在MRI中的百万倍。由于磁性信号的高穿透性,可以真正的看的见磁性探针在全身的各处的分布,其产生的成像信号不会受到组织影响的而衰减。重要的是,可以看的清极低含量的造影剂(5 ng),其灵敏度远高于MRI(Nat. Biomed. Eng., 2020, 4, 325-334)。
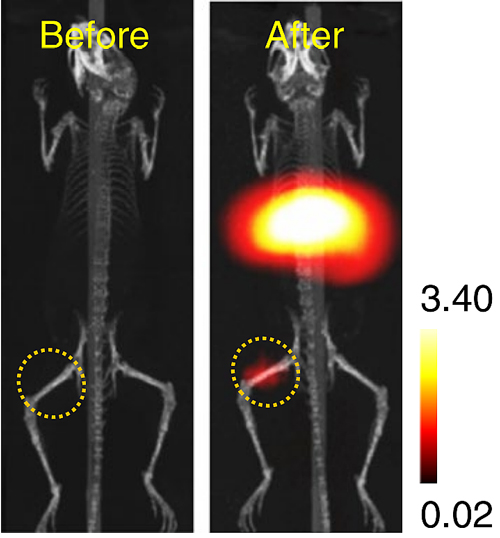
图12. 注射FeCo@C-PEG纳米颗粒前后小鼠的3D MPI-CT图像。
(3)磁性粒子成像综述
磁性示踪剂的设计与合成是磁性粒子成像研究的重点,磁性粒子成像的分辨率与灵敏度和磁性纳米颗粒的性质密切相关。宋国胜教授与斯坦福大学Rao Jianghong教授合作,系统总结了用于MPI成像的磁性粒子合成以及在MPI成像中的应用。总结了示踪剂性能的影响参数,包括尺寸、形状、成分、表面性质、结晶度、应用环境和聚集状态等,为设计更好性能的MPI示踪剂提供指导(图13)。讨论了MPI成像技术在临床转化中的应用及其面临的挑战和前景(Chem. Soc. Rev., 2021, DOI: 10.1039/D0CS00260G)。
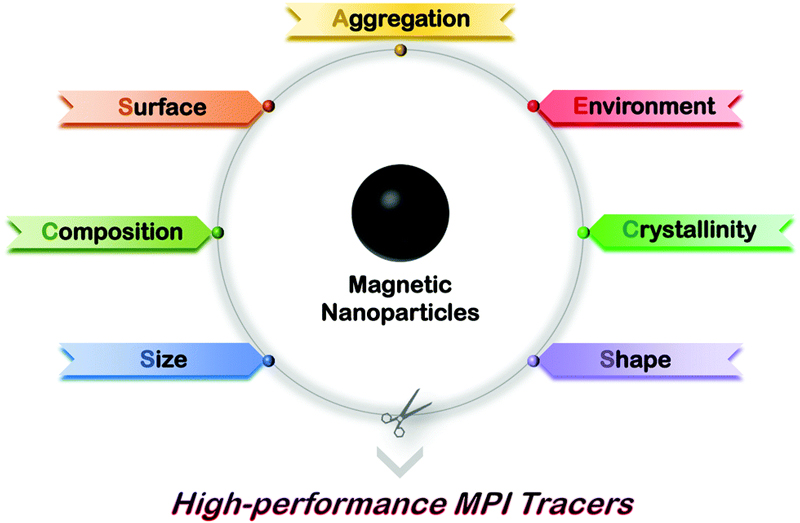
图13. 影响MPI示踪剂性能的因素示意图。
此外,为了实现个性化的治疗和准确的治疗评价,利用成像探针实时准确反映肿瘤治疗进展和疗效的治疗评价策略是非常可取的(图14)。宋国胜实验室综述了磁成像探针和光成像探针在肿瘤治疗评价中的应用现状,以期为实现“量身定制治疗”提供指导。并且简要讨论了实际应用的未来发展和挑战(Coord. Chem. Rev., 2021, 441, 213978)。

图14. 光磁探针用于评价肿瘤治疗的策略。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号