全合成Science:氧化光环化集群式合成苔藓虫生物碱
苔藓虫门是结构多样化卤代次生代谢产物的丰富来源。1996年,Christophersen等人表征了来自苔藓虫Securiflustra securifrons提取物的securamine A(1)和B(2)结构(图1A),并证明了securamine A(1)和B(2)会可逆且溶剂依赖性地异构化为大环内酰胺吲哚衍生物securine A(7)和B(8)。随后,化学家发现了具有细胞毒性的六环双(胺缩醛)分离物securamine D(3)和C(4)以及在C2-C3连接处氧化态不同(如:securamine G(5))或吲哚啉上卤化模式不同(如:securamine I(6))的相关分离物。自20世纪90年代以来,许多课题组致力于合成securamines和相关的chartellines,但是securamines还尚未实现化学合成,而chartelline C(9)由Baran和Shenvi在2006年合成(图1B)。此外,Baran和Nishikawa在先前的研究中通过C20位吲哚的顺序氧化和氮杂邻亚甲基苯醌中间体(10)的重排构建了螺环β-内酰胺,从而可能模拟chartelline C(9)的生物合成。如图1C所示,2,3-二取代吲哚与单线态和三线态分子氧反应会形成3-hydroperoxyindolenines,后者在N1与C12加成后可转化为氮杂邻亚甲基苯醌。另一方面,Wasserman和Foote的基础研究证实将单线态分子氧加成到咪唑中会得到一种endo-过氧化物,再经历开环得到亲电的酰亚胺11(图1D)。在生物系统中,单线态分子氧可以通过酶促或光激发的芳香族氨基酸、卟啉或芳香烃的能量转移形成,这意味着securine A(7)和B(8)关环形成相应的securamines(1和2)后可以掩蔽活性吲哚残基并将氧化转移到溴咪唑上(图1E),进而得到securamine D(3)和C(4)。
近日,美国耶鲁大学的Seth B. Herzon教授(点击查看介绍)课题组发展了一种新颖的方法来实现securamine和securine生物碱家族8个成员(代表3种骨架类型)的全合成。通过高级叠氮化物38和49的模块化组装(13步,产率:6-10%)、顺序氧化光环化和后期官能团化,以17-19步、12-13次纯化以及0.5-3.5%的总产率获得所需产物。其逆合成分析如下(图1F):首先,作者将N5-苄氧甲基(BOM)securamine A(14)作为3种骨架类型的共同前体,它可以通过异构体α,β-不饱和γ-内酰胺15的环化异构化衍生而来,15则能通过酸介导的氯化、12元环内酰胺16的骨架重塑和硝基芳烃的还原得到,而大环内酰胺16可由β-羰基膦酸酯17、醛18和碘乙酰胺19的汇聚式合成获得。相关成果发表在Science 上。
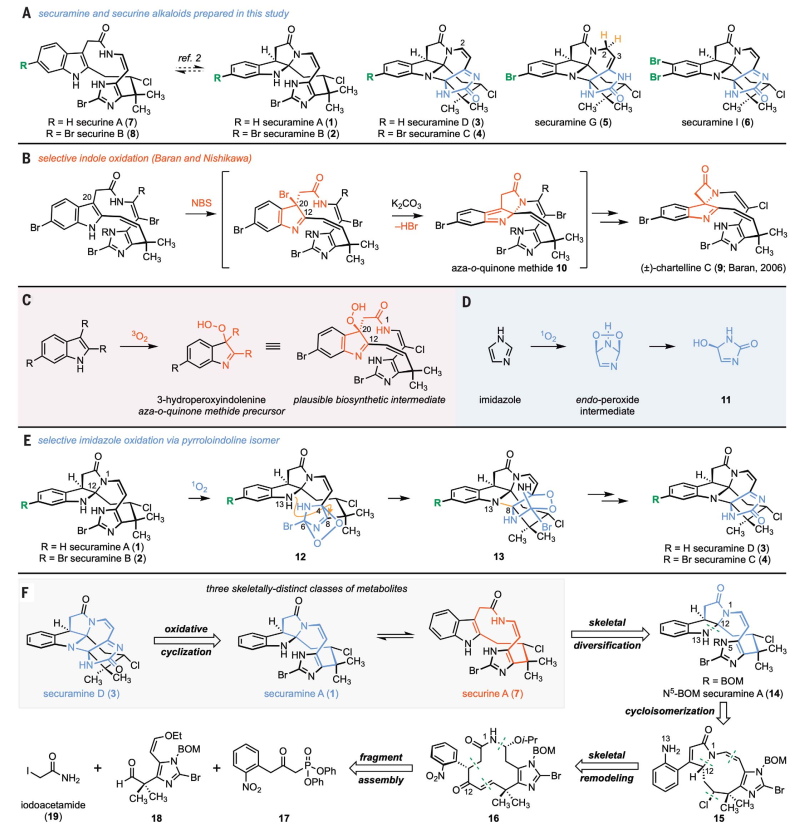
图1. 研究背景及合成计划。图片来源:Science
首先,作者从市售的4-腈甲基咪唑(20)出发,经氢化钠和苄基氯甲基醚(BOMCl)处理后得到N1-和N3-BOM衍生物的混合物(1H NMR分析显示N1:N3-烷基化≈1:2),将该混合物与亚化学计量的苄基氯甲基醚进行加热后可异构化为更稳定的N1-BOM异构体21(产率:80%),并且这一转化可以10 g级规模进行制备(产率:60%)。随后,21经双甲基化反应、位点选择性溴化、Stille交叉偶联反应、C2位去质子化-溴化和氰基还原便可得到醛18(图2A),后者与β-羰基膦酸酯17(由2-硝基碘苯经3步制备而成,产率:51%)在Masamune-Roush烯化条件下进行反应得到α,β-不饱和酮26(单一的(E)-非对映异构体),26通过烯醇醚水解、碘乙酰胺19加成以及碱介导的环化反应得到大环内酰胺28(非对映体比例为19:1),并且C2和C20中心的相对构型通过NOE分析与分子动力学模拟来确定。接着,将28溶解在无水盐酸-二恶烷(4.0 M)中并于23 ℃进行反应便可合成非对映异构体29,其具体过程如下(图2B):28经异丙氧基取代基的初始取代得到中间体30,经烯酮氢氯化(30→31)、HCl消除(31→32)、缩环反应(32→33)、互变异构(33→34)和C12位质子化便可得到产物29,从而一步法构建securamines中四个具有挑战性的亚结构——cis-烯酰胺、新戊基烷基氯、γ-内酰胺和九元环。由于中间体28和29难以分离纯化,因此作者在没有纯化的情况下对硝基芳烃的选择性还原进行了改进,最终以3步、49%的产率和>20:1 d.r.值获得内酰胺15,再通过异构化和关环反应便可能得到N5-BOM securamine A(14),不过不走运的是,咪唑/苯胺的碱性导致该过程无法实现。为此,作者用TBSOTf和2,6-二甲基吡啶处理15并得到甲硅烷氧基取代的吡咯36(图2C),再在四氯化锡的作用下于-78 ℃进行反应获得β,γ-不饱和γ-内酰胺37、15和12-epi-15的混合物(三者比例为3:2:1)。用Lewis/Brønsted酸诱导37环化形成15,而且作者发现12-epi-15在二氯甲烷-d2(23 ℃)中静置后会自发异构化为15,这说明15是热力学上有利的立体异构体。
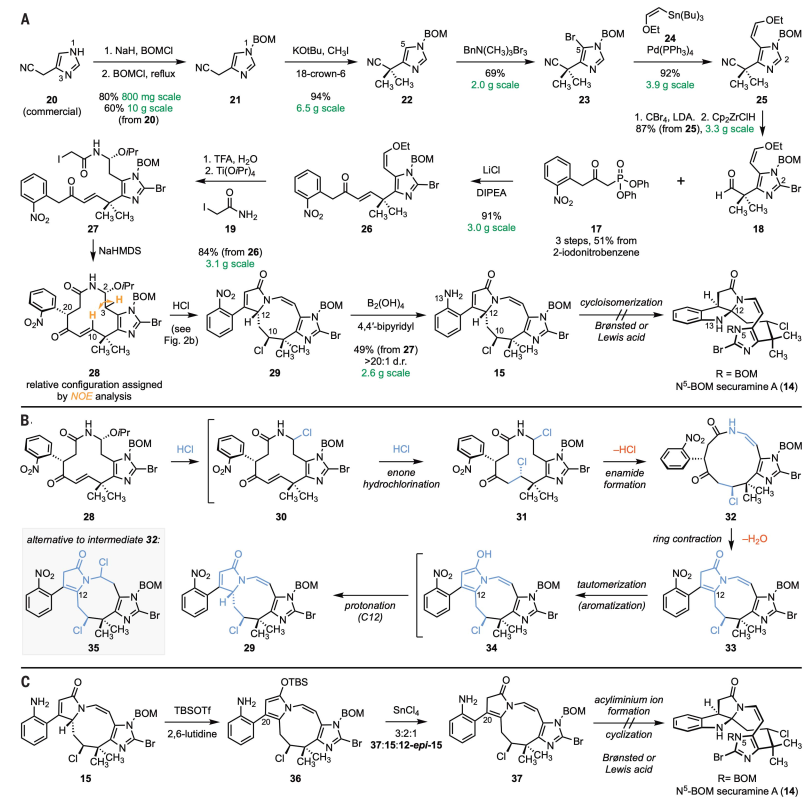
图2. securamine A(1)和securine A(7)前体的合成路线。图片来源:Science
接下来,作者试图通过C-H键胺化形成N13-C12键以获得cis-稠合的吡咯并吲哚啉骨架(图3A)。为了使这种转化可行,C12-H键和N-芳基氮宾必须位于内酰胺的同一面上,因此需要对不饱和γ-内酰胺15进行选择性还原。当用Crabtree’s催化剂和氢气处理15时得到了氢化产物的单一非对映异构体,后者与4-硝基苯甲酰氯反应以79%的总产率获得乙酰苯胺39。尽管NMR分析表明还原反应以所需的立体选择性进行,但是作者通过多次尝试却未能获得39的单晶结构。为此,作者利用微晶电子衍射(MicroED)证实了乙酰苯胺39具有所提出的C-H键胺化所需的相对构型,同时还表明BOM醚在固态中占据了四个构象,进而解释了39的单晶无法均匀生长。另外,作者还通过15的氢化、tBuONO和TMSN3处理获得叠氮化物38(总产率64%、>20:1 d.r.值、800 mg规模),38溶于二氯甲烷中并用紫外光进行照射,以43%的产率、5:1 Z:E比获得N5-BOM securamine A(14),接着在三氯化硼的作用下脱除BOM醚,同时将吡咯并吲哚啉开环为吲哚便可实现securine A(7,总共17步、12次纯化、总产率3.0%)的全合成,而且NMR光谱证实天然和本文合成的securine A(7)数据相一致。尽管Christophersen报道了天然securine A(7)溶于氘代氯仿中会异构化为securamine A(1),但是作者观察到谱线增宽且没有吡咯并吲哚啉骨架的特征。有趣的是,作者将反应步骤调整后(即38先经三氯化硼处理,再用紫外光进行照射)便可以17步、12次纯化、1.4%的总产率获得securamine A(1),并且其光谱数据与天然securamine A(1)一致。值得一提的是,本文合成的securamine A(1)在23 °C的DMSO-d6中十分稳定,当升温至90 °C时,作者观察到1近定量异构化为securine A(7),这与密度泛函理论(DFT)计算相一致,即securamine A(1)的稳定性比securine A(7)低超过4 kcal/mol。总之,这些结果表明securamine A(1)在动力学上是稳定的,并且其开环异构化为securamine A(7)是不可逆的。

图3. 集群式全合成。图片来源:Science
如图3B所示,作者将N5-BOM securamine A(14)和玫瑰红的甲醇溶液置于氧气氛围下进行照射时得到了脒基溴化物45和咪唑啉酮46的混合物(两者比例为1:1.6),并且两种产物的C2位均含有甲醇。由于46中的甲基醚在NMR分析和纯化过程中会不同程度地被水取代(46→47),因此作者将45和46的混合物直接用三氯化硼处理便可提供securamine D(3,总共18步、12次纯化,总产率2.7%),并且其NMR光谱数据与天然securamine D(3)相吻合。另外,作者从醛18出发,经6步转化、24%的总产率合成C16-溴苯胺48,再经还原和重氮转移以两步、64%的总产率获得叠氮化物49(图3C),接着脱除BOM保护基、C-H键胺化便可以17步、12次纯化、1.8%的总产率获得securamine B(2),2通过直接光氧化反应可转化为securamine C(4,总共18步、12次纯化,总产率1.4%),其分别通过还原和溴化反应便可得到securamine G(5,总共19步、13次纯化,总产率0.7%)和securamine I(6,总共19步、13次纯化,总产率0.5%)。或者,49先进行C-H键胺化再脱除保护基便能以17步、12 次纯化、3.5%的总产率实现securine B(8)的全合成,并且securamine B(2)、securamine I(6)和securine B(8)的光谱数据与天然产物一致。
总结
Seth B. Herzon教授课题组通过叠氮化物38和49的模块化组装(13步,产率:6-10%)、顺序的氧化光环化反应和后期官能团化反应,以17-19步、12-13次纯化以及0.5-3.5%的总产率实现了Securiflustra securifronss生物碱家族8个成员的全合成。此外,作者还通过微晶电子衍射(MicroED)分析阐明了高级中间体乙酰苯胺的结构。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

An oxidative photocyclization approach to the synthesis of Securiflustra securifrons alkaloids
Brandon W. Alexander, Noah M. Bartfield, Vaani Gupta, Brandon Q. Mercado, Mark Del Campo, Seth B. Herzon
Science. 2024, 383, 849-854, DOI: 10.1126/science.adl6163
导师介绍
Seth B. Herzon
https://www.x-mol.com/university/faculty/1291
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号