南京大学黄硕团队Nat. Commun.:纳米孔快速水果分析
顺式二醇,如1,2-二酚、糖醇、α-羟基酸及糖 [1-4] 等,广泛存在于日常生活中的天然食品中,如水果、茶叶、蜂蜜和蔬菜等。这些物质对人体健康至关重要,它们不仅提供必需的营养成分 [5],还具有多种保健功能,包括并不限于抗氧化 [6]、抗肿瘤 [7] 以及降血压 [8] 等。因此,对这些顺式二醇的快速而精确的分析对于保障人们的饮食营养和保健非常关键,同时也对食品工业中产品的安全性和质量控制起到了核心作用。然而,由于这些天然来源的顺式二醇在未经分离的情况下通常以混合物形式存在,这就对单一传感器在同一条件下快速准确鉴别这些化合物提出了严峻的技术挑战 [9]。
传统的高效液相色谱技术(HPLC)长期以来一直是分析天然食品中顺式二醇的主流方法 [9],但其所需的样品预处理步骤繁复耗时,且设备体积较大,限制了其在现场快速分析的应用。此外,当需要在同一色谱条件下同时检测多种分析物时,HPLC面临着不同物质可能存在共洗脱的挑战 [10],进而影响分析结果的准确性和可靠性。其他常用的分析方法如分光光度法 [11]、气相色谱法 [12] 等则因其分辨率不足或需要衍生化的复杂操作,难以实现快速准确分析顺式二醇的目的。鉴于此,开发一种无需复杂分离且能快速准确地同时识别多种顺式二醇的分析方法,是食品科学及化学分析领域亟待解决的问题。
近日,南京大学化学化工学院黄硕教授(点击查看介绍)课题组利用单个苯硼酸修饰的异质耻垢分枝杆菌膜蛋白A(MspA)孔道(MspA-PBA),首次实现了天然水果中多达十多种顺式二醇的同时快速准确分析,且无需依赖任何繁琐的分离纯化步骤。在该工作中,MspA-PBA展现出优异的高分辨能力,能够同时完全分辨多达12种顺式二醇,包括同分异构体柠檬酸和异柠檬酸,果糖和葡萄糖,以及对映异构体DL-苹果酸。该传感器在西梅、葡萄、柠檬、不同品种猕猴桃以及商业果汁产品中均表现出色,并可被直接应用于便携式设备进行现场快速检测。该工作中,作者提出了基于MspA-PBA的多特征纳米孔谱技术概念,并选取了四大类共十种在自然界中常见的顺式二醇作为目标分析物建立机器学习模型(图1),包括儿茶素(CAT)、新绿原酸(3-CQA)、山梨糖醇(D-SOR)、木糖醇(XYL)、L-苹果酸(L-MA)、L-酒石酸(L-TA)、柠檬酸(CA)、异柠檬酸(ICIT)、葡萄糖(D-GLC)和果糖(D-FRU),机器学习识别准确率达99.3%。得益于MspA孔道卓越的空间分辨率,同分异构体柠檬酸和异柠檬酸,葡萄糖和果糖分别报告出差异显著的纳米孔信号,充分证明了基于纳米孔水果分析的可行性。
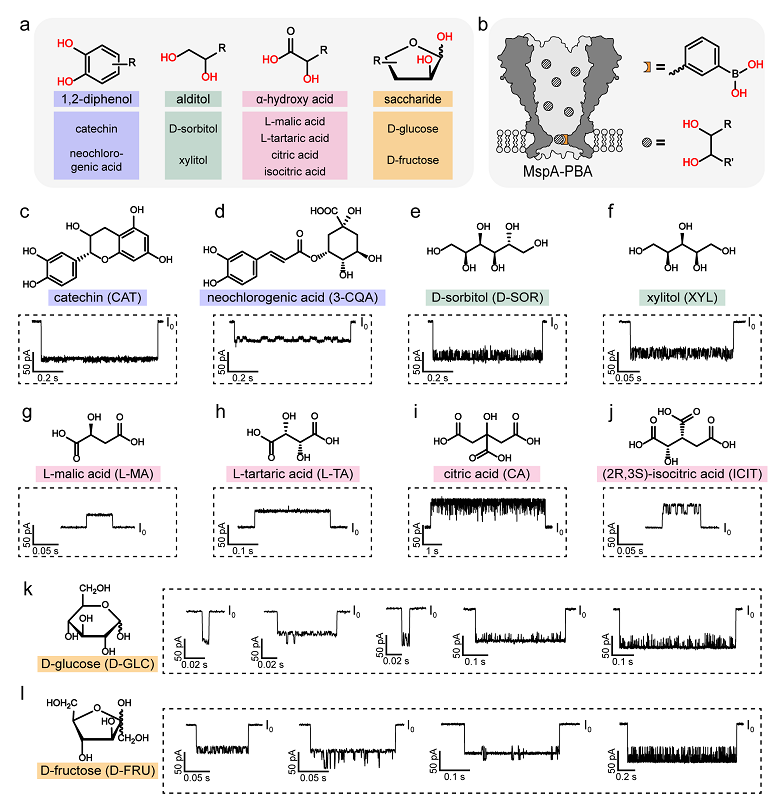
图1. 目标顺式二醇的直接传感
通过借助机器学习算法,作者深入研究了西梅、葡萄和柠檬中顺式二醇的含量(图2)。结果显示,每种水果所呈现出的纳米孔信号具有鲜明的差异,如西梅中特有的山梨糖醇和新绿原酸,葡萄中的酒石酸以及柠檬中的柠檬酸和异柠檬酸。这是纳米孔技术在水果分析领域的首次成功应用,充分证明了MspA-PBA在检测复杂样品时的巨大潜力。这些检测结果中的差异也为进一步理解不同水果中顺式二醇成分的生物学功能及其在食品科学中的应用价值开辟了新的视角。
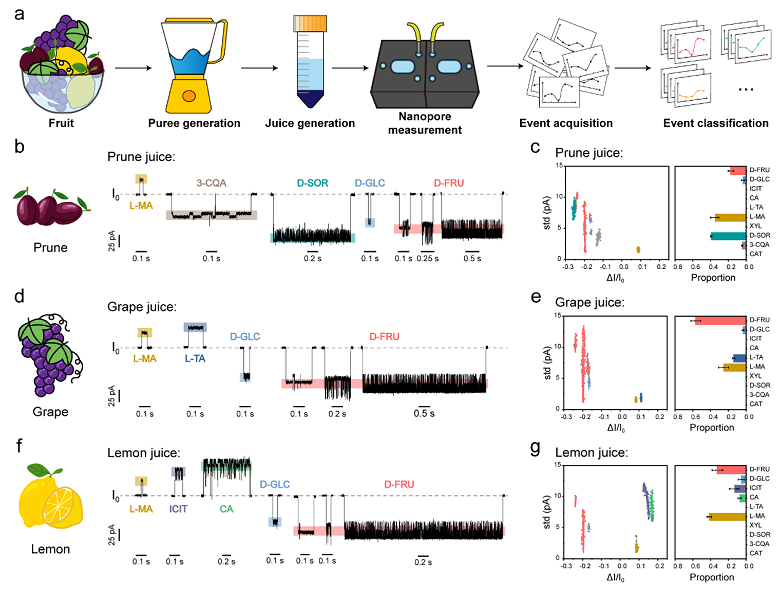
图2. 天然水果果汁的快速分析
随后,作者将相同的分析策略应用于不同品种的猕猴桃研究中,并利用相关文献及算法成功鉴定出了绿心和黄心猕猴桃特有的蔗糖信号以及红心猕猴桃中未知种类的顺式二醇信号(图3)。此外,该技术在商品果汁中的添加剂鉴定方面也取得了进展,DL-苹果酸这一对映异构体可被同时完全区分。最终,作者将该传感器集成于便携式设备中,成功实现了天然葡萄汁的实时传感分析,进一步展示了该方法在便携式食品和药品检测领域的广阔应用潜力,极大地推动了纳米孔技术向实际场景应用的转变。
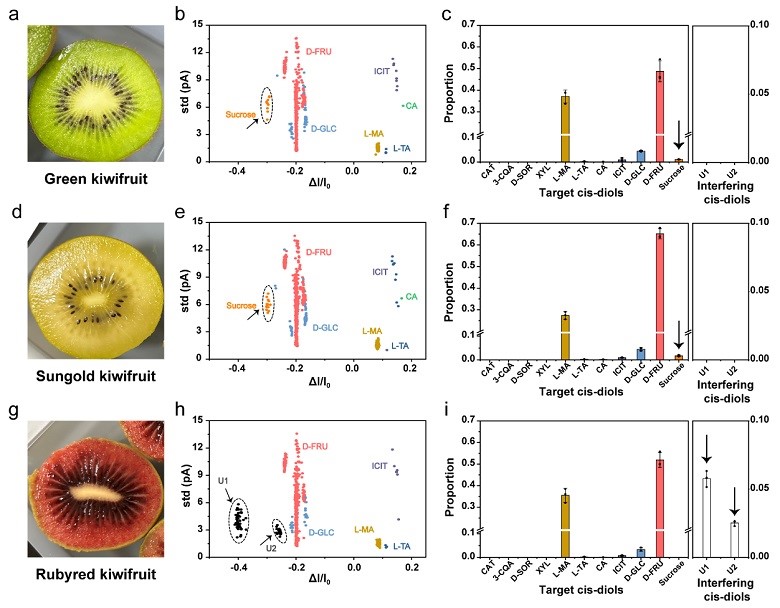
图3. 不同品种猕猴桃的快速分析
该工作于近日发表在Nature Communications,南京大学化学化工学院黄硕教授为该论文的通讯作者。南京大学博士生樊萍萍为该论文第一作者,科研助理曹祯媛和博士生张善雨为等同贡献第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nanopore analysis of cis-diols in fruits
Pingping Fan#, Zhenyuan Cao#, Shanyu Zhang#, Yuqin Wang, Yunqi Xiao, Wendong Jia, Panke Zhang & Shuo Huang*
Nat. Commun., 2024, 15, 1969. DOI: 10.1038/s41467-024-46303-x
参考文献
1 Tiitinen, K. M., Yang, B., Haraldsson, G. G., Jonsdottir, S. & Kallio, H. P. Fast analysis of sugars, fruit acids, and vitamin C in sea buckthorn (Hippophae rhamnoides L.) varieties. J. Agric. Food Chem. 54, 2508-2513.
2 Fang, T. et al. Analysis of sorbitol content variation in wild and cultivated apples. J. Sci. Food Agric. 100, 139-144.
3 Al-Farsi, M. et al. Quality evaluation of Omani honey. Food Chem. 262, 162-167.
4 Issaoui, M. et al. Phenols, Flavors, and the Mediterranean Diet. J. Aoac. Int. 103, 915-924.
5 Malongane, F., McGaw, L. J. & Mudau, F. N. The synergistic potential of various teas, herbs and therapeutic drugs in health improvement: a review. J. Sci. Food Agric. 97, 4679-4689.
6 Yilmaz, Y. & Toledo, R. T. Major Flavonoids in Grape Seeds and Skins: Antioxidant Capacity of Catechin, Epicatechin, and Gallic Acid. J. Agric. Food Chem. 52, 255-260.
7 Rawangkan, A. et al. Green Tea Catechin Is an Alternative Immune Checkpoint Inhibitor that Inhibits PD-L1 Expression and Lung Tumor Growth. Molecules 23, 2071.
8 Erejuwa, O. O., Sulaiman, S. A. & Wahab, M. S. Fructose might contribute to the hypoglycemic effect of honey. Molecules 17, 1900-1915.
9 Akagic, A. et al. Geographic Variability of Sugars and Organic Acids in Selected Wild Fruit Species. Foods 9, 462.
10 Eyéghé-Bickong, H. A., Alexandersson, E. O., Gouws, L. M., Young, P. R. & Vivier, M. A. Optimisation of an HPLC method for the simultaneous quantification of the major sugars and organic acids in grapevine berries. J. Chromatogr. B 885-886, 43-49.
11 Jiang, C. C., Fang, Z. Z., Zhou, D. R., Pan, S. L. & Ye, X. F. Changes in secondary metabolites, organic acids and soluble sugars during the development of plum fruit cv. 'Furongli' (Prunus salicina Lindl). J. Sci. Food Agric. 99, 1010-1019.
12 Zhou, Y. et al. Fruit sugar and organic acid were significantly related to fruit Mg of six citrus cultivars. Food Chem. 259, 278-285.
导师介绍
黄硕
https://www.x-mol.com/university/faculty/56491
课题组网站
http://hysz.nju.edu.cn/bionano
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号