赵晓丹教授课题组JACS:铜催化烯烃的对映选择性亲电胺化/双官能团化反应
烯烃是一类常见的化合物,它们的结构单元广泛存在于药物分子、天然产物的分子中。烯烃的亲电双官能团化反应为它们的转化提供了一条重要的途径。通过这种方式,能够快速地向烯烃分子引入一个亲电基团和一个亲核基团,合成其它方式难以构建的化合物。从机理上讲,这一类反应是由高活性的亲电试剂引发,与烯烃形成三元环鎓离子中间体,随后被外来的或者分子自身连接的亲核基团进攻开环,生成最终的双官能团化产物。2010年以来,通过这种反应模式,实现了各类催化烯烃不对称亲电双官能化反应,如烯烃的不对称亲电氯化、溴化、碘化、硫化和硒化反应等(图1a, 左)。相比而言,由于氮亲电试剂反应性的问题及直接形成环氮鎓离子的困难性,普通烯烃的不对称亲电胺化双官能团化反应鲜有报道,实现这一反应具有大的挑战性(图1a, 右)。
中山大学化学学院赵晓丹教授(点击查看介绍)课题组近年来一直致力于烯烃的不对称双官能团化反应的研究,通过使用课题组开发的双功能硫属化合物手性催化剂,实现了烯烃系列的不对称双官能团化反应,如不对称三氟甲硫基化、烷硫基化、芳硫基化、氯化和碘化反应(Acc. Chem. Res. 2022, 55, 2439-2453; J. Am. Chem. Soc. 2022, 144, 16490-16501)。发展不对称的亲电胺化双官能团化反应成为该课题组下一个重要的研究目标。最近,该课题组发现,采用金属控制的方式,能够实现烯烃的不对称亲电胺化双官能团化反应(图1b)。在该反应中,Cu(NTf2)2作为强的Lewis酸,活化偶氮二甲酸酯试剂,使其形成高活性的亲电氮物种,在新发展的氰基噁唑啉手性配体的配合下,能够与烯烃的π键结合,高对映选择性地形成三元环氮鎓离子中间体,进而完成[3+2]和分子内环化转化。该反应化学选择性、区域选择性、对映和非对映选择性好,且亲核基团的范围宽泛。
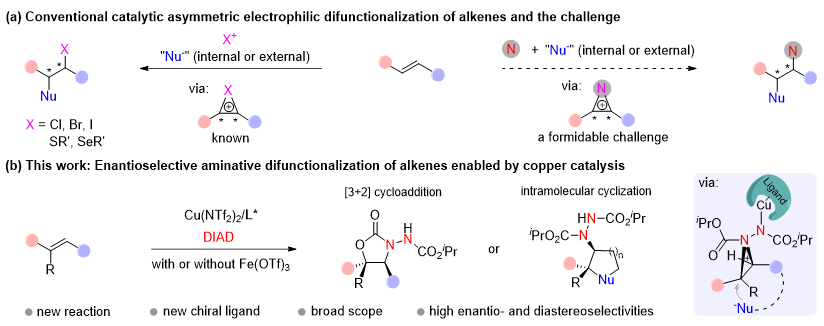
图1. 烯烃的催化不对称亲电双官能化反应
在取得最优的反应条件后,作者对底物范围进行了考察(图2和3)。在[3+2]环加成的反应中,在烯烃底物一侧的烷基基团上引入各种官能团或者延长碳链,反应均可以较好的收率和高对映选择性生成目标产物。在改变烯烃的芳基取代基时发现,供电子芳基可产生更好的结果,而连接有相对缺电子的芳基时,产率有所下降。对于分子内环化反应,反应效果好,不同的亲核性基团,如醇、酚、羧基、酰胺基、富电子芳基均可作为亲核基团。遗憾的是,由于1,2-二烷基烯烃的活性较低,在该反应体系中并不能生成相应的双官能团化的目标产物。
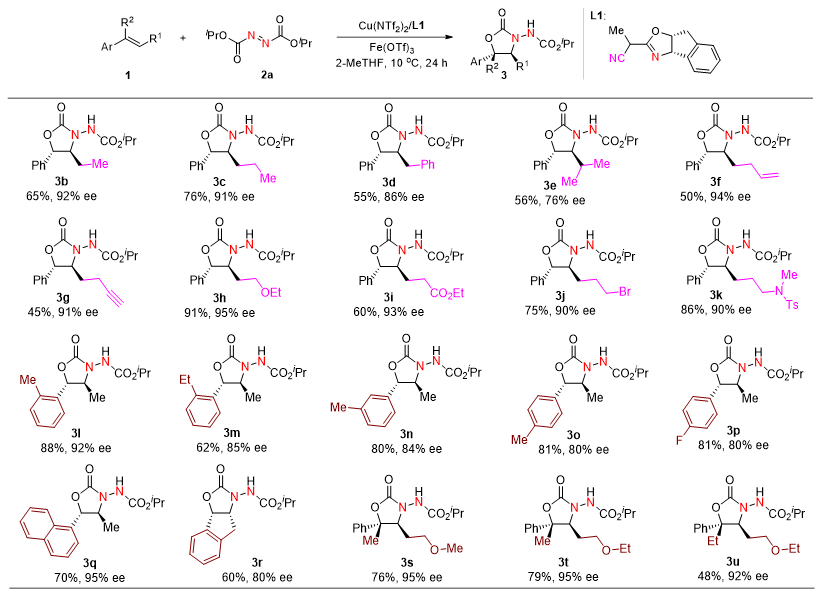
图2. 铜催化烯烃的不对称[3+2]环加成反应
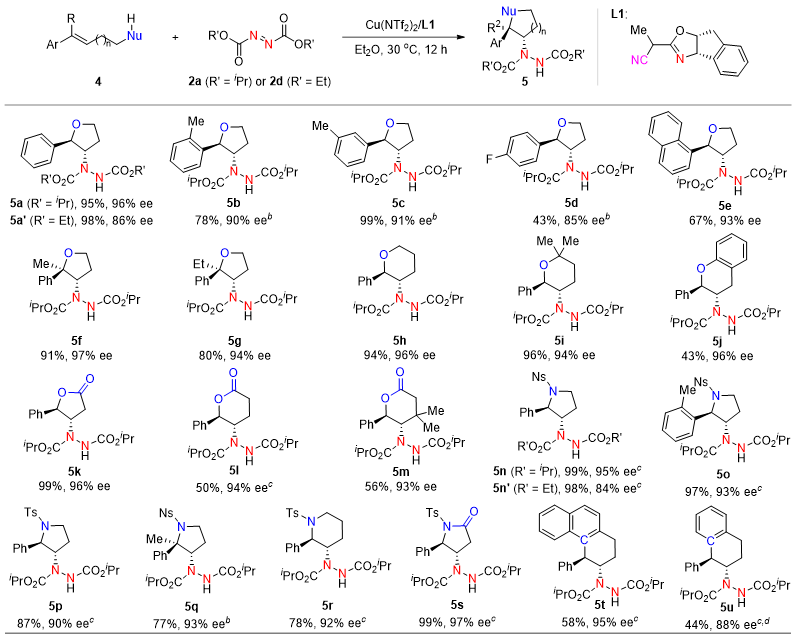
图3. 铜催化烯烃的不对称亲电胺化分子内环化反应
随后,作者对合成得到的手性噁唑烷酮和含肼杂环进行了简单转化(图4),可以制备得到如硫代噁唑烷酮衍生物等等有价值的化合物,从而证明了该方法的应用潜在价值。
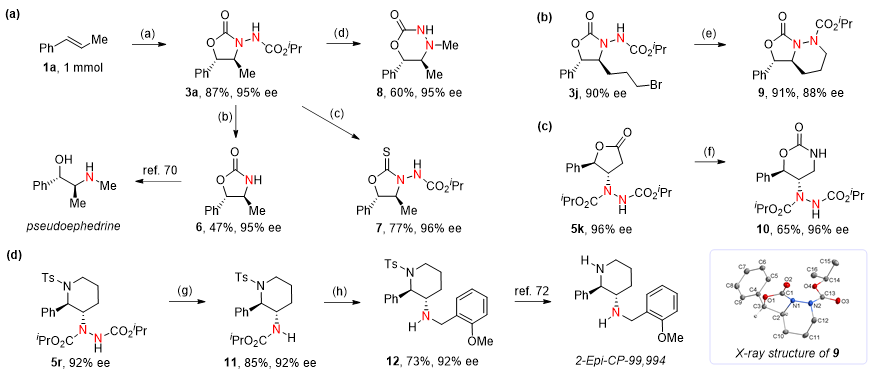
图4. 反应所得环化产物的衍生转化研究
最后,为了了解该反应的机理,作者进行了控制实验等方面的研究,根据其结果,作者提出了可能的反应机理:首先Cu(NTf2)2与手性配体L配位形成手性的铜配合物I。所形成的铜络合物可活化偶氮二羧酸酯2a以产生亲电的氮物种II。高活性的II诱导烯烃π键选择性地与其结合得到手性氮鎓离子中间体III。然后,中间体III被亲核试剂开环产生目标产物3或5并再生催化剂I(图5)。作者也推测新的手性配体与金属中心结合的方式,及反应中为何有时需要加入铁盐。
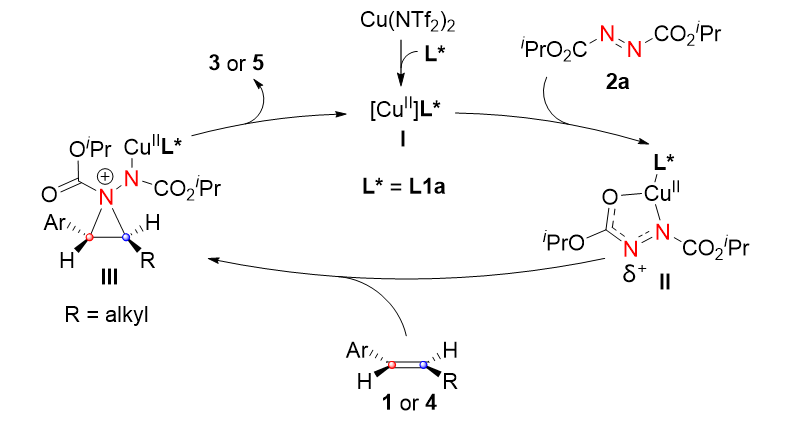
图5. 反应可能的机理
综上,该研究利用金属活化的策略,实现了烯烃的不对称胺化双官能团化反应,合成了一系列光学纯的肼类衍生物,为含氮手性分子的构建提供了新的途径。另外,该研究揭示了亲电的氮,作为一种硬酸,与烯烃能够直接结合形成手性的氮鎓离子。重要的是,也报道了一种新的手性配体,这种配体在其它的催化反应中可能有应用的潜在。相关研究成果近期发表在J. Am. Chem. Soc.上,中山大学博士研究生黄楠为论文的第一作者,中山大学赵晓丹教授为通讯作者。上述研究得到了国家自然科学基金等的经费支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Catalytic Enantioselective Aminative Difunctionalization of Alkenes
Nan Huang, Jie Luo, Lihao Liao, and Xiaodan Zhao*
J. Am. Chem. Soc., 2024, 146, 7029–7038, DOI: 10.1021/jacs.4c00307
导师介绍
赵晓丹
https://www.x-mol.com/university/faculty/15401
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号