共价药物新舞台——瞄准赖氨酸的共价药物开发
共价药物一百多年前就已出现,例如大名鼎鼎的阿司匹林与青霉素,它们的乙酰水杨酸基团以及β-内酰胺四元环,可以与靶标蛋白上的亲核基团产生共价反应,从而以更牢固的共价方式结合受体。这意味着与非共价药物相比,它们具有更长的作用时间,并且能够在更小的剂量下发挥药效。近年来,共价药物因其效力和能力而越来越受到药物开发人员的关注。大名鼎鼎的治疗套细胞淋巴瘤的依鲁替尼(ibrutinib)和抗SARS-CoV-19药物Paxlovid中的活性成分nirmatrelvir都是共价药物(图1)。
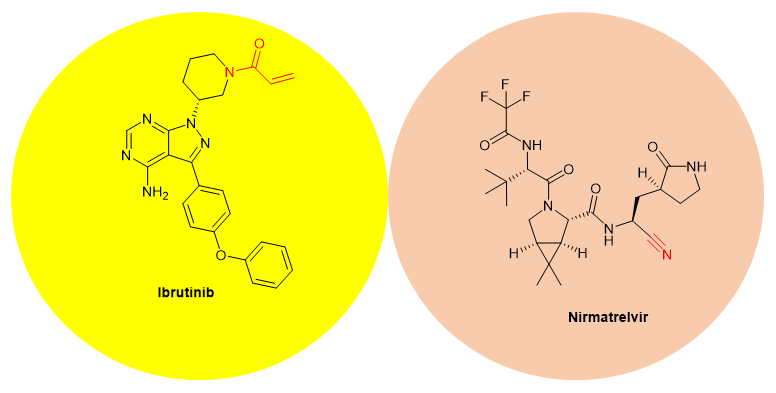
图1. Ibrutinib和nirmatrelvir化学结构。
共价药物通常带有一个亲电基团,可以与受体蛋白上丰富的亲核基团产生共价反应,因此共价药物上的这个反应活性基团,也被形象地成为“弹头(Warhead)”,例如irutinib和nirmatrelvir上的亲电弹头就分别是丙烯酰胺与氰基。从蛋白受体的角度来看,氨基、羟基、甲巯基、巯基、咪唑基等亲核基团,都可以成为共价药物靶向的基团。其中,半胱氨酸巯基丰度较低,在众多适应症中发挥重要的生理学作用,而且去质子后巯基具有高度的亲核性,因而成为了绝大多数共价药物靶向的目标。Ibrutinib和nirmatrelvir均靶向受体上的关键半胱氨酸,前者瞄准的是布鲁顿酪氨酸激酶(BTK)上的Cys481;后者则靶向SARS-CoV-19病毒的3C样蛋白酶(3CLPRO)上的Cys145。
尽管半胱氨酸因其上述特性成为了绝大多数共价药物靶向的基团,但仍然存在非半胱氨酸的氨基酸靶标,为其它的共价药物的开发提供了思路,例如在蛋白组中大量存在的赖氨酸。半胱氨酸作为共价结合位点尽管取得了很大的成功,但却存在不小的挑战。一方面,它具有一定程度的选择性——人体蛋白质的半胱氨酸的比例很小,因此可以实现较高的选择型和较低的脱靶效应。另一方面,由于半胱氨酸较低的丰度,使得靶向半胱氨酸的策略不能“放之四海而皆准”地适应共价药物的开发。与半胱氨酸不同,赖氨酸在蛋白质中广泛存在,它侧链的氨基同样具有较强的亲核性(尽管在生理条件下,大多数赖氨酸氨基被质子化),从这个角度来看,赖氨酸有望使更多人类蛋白质可用于靶向共价药物。赖氨酸残基的数量几乎是体内半胱氨酸的三倍,平均每种蛋白质大约包含32个赖氨酸残基。
半胱氨酸靶向共价药物的研究还发现,某些与癌症相关的蛋白质(例如表皮生长因子受体EGFR)可以产生突变,以将其关键的被靶向的半胱氨酸残基转换为其他氨基酸,从而使曾经的母体蛋白靶标不再被药物靶向,实现所谓的耐药性。与之相反,靶向赖氨酸的药物被卷入耐药性问题的可能性较低。这是因为对于某些大类蛋白质(例如激酶中),赖氨酸对蛋白质的功能至关重要,无法用另一种氨基酸代替。作为药物靶标,赖氨酸不仅用途广泛,而且产生耐药性的问题较少。尽管如此,专家仍然认为,靶向赖氨酸的共价药物开发至少要落后半胱氨酸十年以上。目前尚无靶向赖氨酸的共价药物上市,而靶向半胱氨酸的共价药物例如ibrutinib和osimertinib,不仅成功上市,而且在一定程度上制定了共价药物开发的基调。

图2. Osimertinib化学结构。
赖氨酸的潜力
尽管赖氨酸在蛋白质中普遍存在,但并非所有赖氨酸都可以作为药物的靶点。当暴露在酸性甚至弱碱性环境中时,例如生理 pH 值时,赖氨酸的侧链氨基都会质子化,不再具备亲核性。因此,药物开发通常会注重那些蛋白质内部赖氨酸,尤其是具有较低pKa的赖氨酸残基,它们可能会以中性而非质子化的氨基形式存在。
为了探索赖氨酸的潜力范围,研究人员最近绘制了人类蛋白质中赖氨酸的分布图,以寻找可成药的位点。他们的努力表明,在这个相对未开发的领域存在大量机会。康奈尔大学化学家 Mikail Abbasov 及其同事梳理了人体蛋白质可靶向赖氨酸的免疫细胞和癌细胞。[1] 研究人员绘制了超过 14,000 个赖氨酸,其中至少有 3,000 个可以用于开发共价药物。该小组还进行了实验,以评估各种反应基团在不同位点与赖氨酸共价结合的效率,为共价药物设计提供起点。
共价/非共价相得益彰
赖氨酸的亲核性比半胱氨酸较低,因此可能需要活性更高的亲电弹头。但从共价药物的角度来看,过强的亲电基团可能会导致药物本身的化学稳定性出现问题(例如含有醛羰基的化合物,其对湿度较为敏感),而且过强的亲电性会导致共价药物的选择性降低,导致它们可能与血液中的水、酶或其他化合物发生反应。开发者因此需要在亲电药物设计中平衡反应性和稳定性。由加州大学河滨分校的 Maurizio Pellecchia 领导的团队已经在这个平衡点的追求过程中取得了显著的进步:他们从高亲电性的磺酰氟开始,通过调整正确的给电子基团来调和它的亲电性。[2] 在另一个案例中,研究人员设计了一种芳基氟磺酸酯(图3),可以与受体上的赖氨酸发生选择性共价结合。[3]

图3. 靶向赖氨酸的含芳基氟磺酸酯的共价药物候选物。
共价药物的亲电弹头不能与药物分子中的其它部分割裂开来,否则单独地合成一个芳基氟磺酸酯岂非就可作为共价药物?图3分子上的多肽部分需要与受体蛋白实现有选择性的非共价作用,将其亲电弹头递送到靶向的赖氨酸附近,从而促进氟磺酸酯与赖氨酸之间的共价反应。抗SARS-CoV-19药物Paxlovid中的活性成分nirmatrelvir,就是依靠这种非共价为基础、共价结合为重点的模式,实现对于3C样蛋白的绑定而使其丧失关键的生物学活性。
共价键的形成与断裂
可逆共价抑制剂也是共价药物发展的一个方向,所谓的可逆并非有机化学层面的可逆,而是指产生的共价键在某种情况下可以断裂。例如nirmatrelvir中,通过分子上的氰基与半胱氨酸巯基之间形成的硫代亚胺酸酯,可以在水解的条件下分裂为巯基和酰胺。它并没有恢复初始的氰基,因此从有机化学家的角度来看,这并非一个可逆反应,而是反应产物继续的降解。但从药理学来看,巯基被恢复,因此受体得到了再生,所以属于可逆过程。
醛基可以靶向赖氨酸氨基,产生可逆共价结合的效果。以醛基为弹头的共价药物已经实现了商业化,例如2019年通过FDA审批的治疗镰状细胞病的voxelotor(图4),就是通过药物分子中的醛基结合血红蛋白上的 N 端氨基实现药效的。
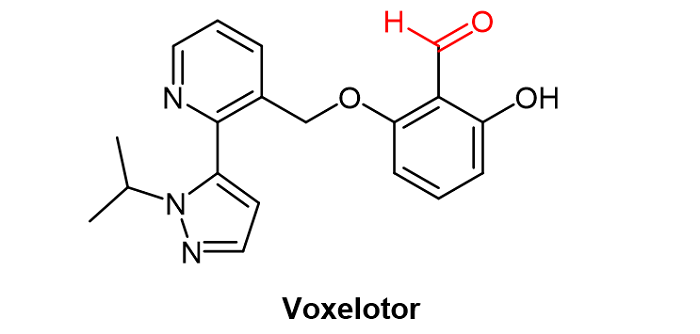
图4. Voxelotor化学结构。
尽管Novartis因为商业原因放弃了voxelotor,但还是开发了可逆共价抑制剂 roblitinib,一种靶向半胱氨酸的含醛基共价药物,并通过了2期临床试验,作为肝癌的潜在疗法。虽然voxelotor和roblitinib都不靶向赖氨酸,但针对赖氨酸的共价药物,似乎离问世不算太遥远了。
靶向赖氨酸的共价药物,任重而道远
制造有效的共价药物需要平衡各种因素,药物分子骨架、亲电基团的选择、恰当的反应活性以及靶标赖氨酸周围的微环境。尽管含量丰富,但赖氨酸并不意味着能够取代半胱氨酸作为首选的共价靶标。相反,研究人员希望半胱氨酸和赖氨酸能够相互补充,以扩大整体可成药空间。[4] 除了赖氨酸之外,丝氨酸与酪氨酸也成为了研究的靶标(丝氨酸实际上已经在阿司匹林的神话里面成功地成为了靶标)。尽管困难重重,但一旦成功,共价药物抑制剂的开发经迎来崭新的舞台。
参考文献
1. Abbasov, M. E. et al. A proteome-wide atlas of lysine-reactive chemistry. Nat. Chem. 2021, 13, 1081–1092.
2. Udompholkul, P. et al. Lysine Covalent Antagonists of Melanoma Inhibitors of Apoptosis Protein. J. Med. Chem. 2021, 64, 16147–16158.
3. Baggio, C. et al. Aryl-fluorosulfate-based Lysine Covalent Pan-Inhibitors of Apoptosis Protein (IAP) Antagonists with Cellular Efficacy. J. Med. Chem. 2019, 62, 9188−9200.
4. Kim, S. E. Looking to lysine. ACS Discovery Report. Q2, 2022.
(本文由北纬55°供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号