Nano Res.[生物]│国家纳米中心王浩、易宇:硒肽原位自组装抑制单核细胞黏附改善动脉粥样硬化
本篇文章版权为王浩课题组所有,未经授权禁止转载。

背景介绍
动脉粥样硬化是一种慢性炎症疾病,可能导致严重的心脑血管疾病,例如心肌梗死和中风。目前针对动脉粥样硬化的药物例如他汀类药物治疗效果有限。在动脉粥样硬化的进展过程中,氧化应激、单核细胞粘附以及分化成炎症巨噬细胞起着重要作用。单核细胞一般通过结合病变血管内皮细胞膜上的黏附分子(例如血管细胞黏附分子-1(VCAM-1)和P-选择素)进行黏附和入侵,然而传统的黏附分子抑制药物存在全身性副作用问题。因此,发展在病理组织中对炎症相关免疫细胞进行精确调控的方法具有重要意义。
成果简介
针对上述问题,国家纳米科学中心王浩研究员、易宇副研究员发展了能够靶向动脉粥样硬化斑块、原位激活抗单核细胞黏附功能的自组装硒肽用于动脉粥样硬化的治疗。该硒肽通过模块化设计理念制备而成,其分子结构包括VCAM-1斑块靶向模块、活性氧(ROS)响应硒氨基酸连接子、以及两条十八烷基疏水链(图1)。通过静脉给药,装载了辛伐他汀的硒肽纳米药物通过靶向递送在动脉粥样硬化斑块组织中高效富集(富集量比无靶向纳米药物提升至2.2倍),并在炎症组织高表达的ROS刺激下释放药物。通过局部消除ROS和释放抗炎药物,巨噬细胞的炎症反应得到缓解。同时,硒肽在炎症活性氧浓度下会发生β-消除化学反应,我们发现其氧化代谢产物十八烷基硒酸能够原位形成纳米胶束并特异性结合P-选择素而抑制单核细胞黏附,其亲和力常数高达1.5μM,比特异性结合P-选择素的肝素(临床抗凝血药物)的亲和力还高3.9倍。这是由于(1)烷基亚硒酸中的亚硒酸基团比肝素中的硫酸基团电负半径更大,与P-选择素结合域中阳离子氨基酸的静电相互作用比肝素更强;(2)自组装带来的多价相互作用增强了结合能力。通过局部抑制单核细胞粘附和抗炎抗氧化,硒肽纳米药物对动脉粥样硬化小鼠模型中斑块抑制效果比单独使用辛伐他汀提升至2.6倍。
图文导读
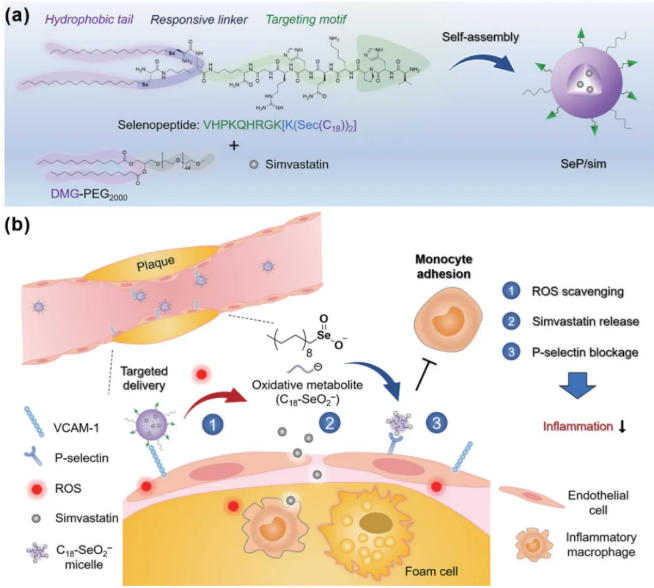
图1. 硒肽通过靶向药物递送和局部调节炎症微环境改善动脉粥样硬化。(a)硒肽的模块化结构及纳米药物制备。(b)硒肽纳米颗粒通过靶向药物递送、抗氧化和抑制单核细胞粘附,抑制动脉粥样硬化的发展。
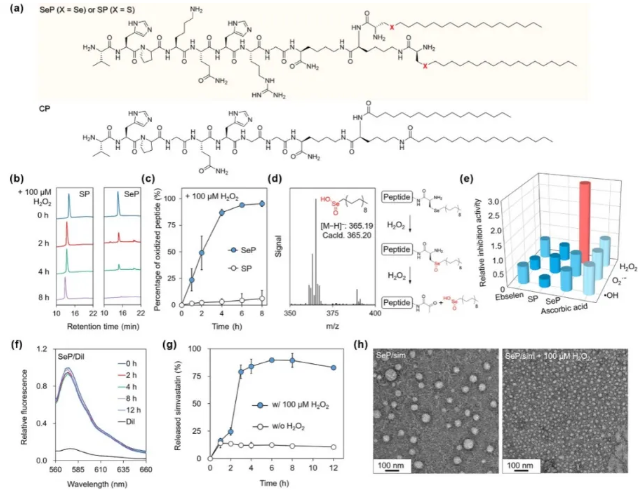
图2.硒肽的理化性质表征。(a)硒肽、硫肽和对照肽的化学结构。(b、c)硒肽和硫肽的氧化响应性比较。(d)硒肽氧化代谢物产物的质谱表征。(e)硒肽对H2O2、O2•ˉ和•OH的清除能力。(f)硒肽纳米颗粒的稳定性测试。(g)硒肽在100 μM过氧化氢条件下释放药物情况。(h)硒肽纳米药物在100 μM过氧化氢氧化前后的TEM图像。
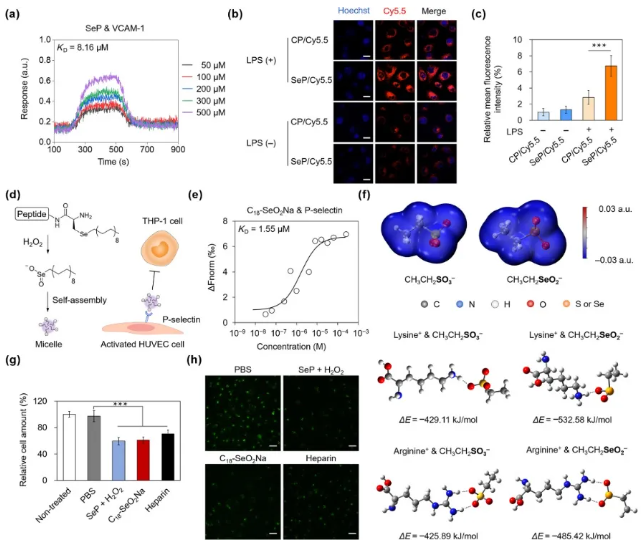
图3.硒肽氧化代谢产物与P-选择素相互作用研究。(a)表面等离子共振(SPR)分析硒肽和VCAM-1之间的亲和力。(b、c)硒肽纳米颗粒对炎症刺激的人脐静脉内皮细胞(HUVEC)的靶向能力表征(刻度:20μm)。(d)十八烷基亚硒酸胶束通过结合P-选择素抑制单核细胞粘附。(e)微量热泳动仪(MST)分析P-选择素和十八烷基亚硒酸钠之间的亲和力。(f)DFT计算CH3CH2SO3‒或CH3CH2SeO2‒与带正电的赖氨酸和精氨酸之间的结合能。(g)人单核细胞(THP-1)在经过了样品处理后的修饰了P-选择素培养皿上的粘附情况。(h)THP-1细胞在经过了样品处理后的炎症刺激HUVEC细胞上的粘附情况(刻度:100μm)。
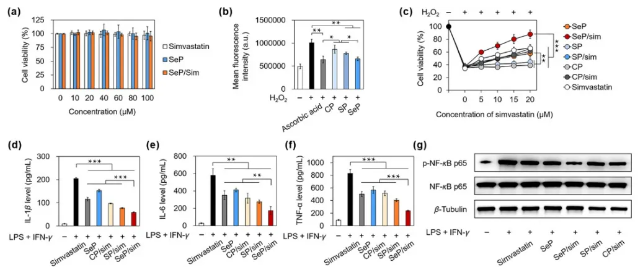
图4.硒肽纳米药物在细胞层面的抗氧化和抗炎活性。(a)硒肽及其纳米药物对HUVEC细胞的细胞毒性评价。(b)硒肽抗氧化能力评价。(c)硒肽纳米药物抗氧化凋亡能力评价。(d-f)硒肽抗炎能力评价。(g)硒肽纳米药物抑制NF-κB信号通路激活的能力。
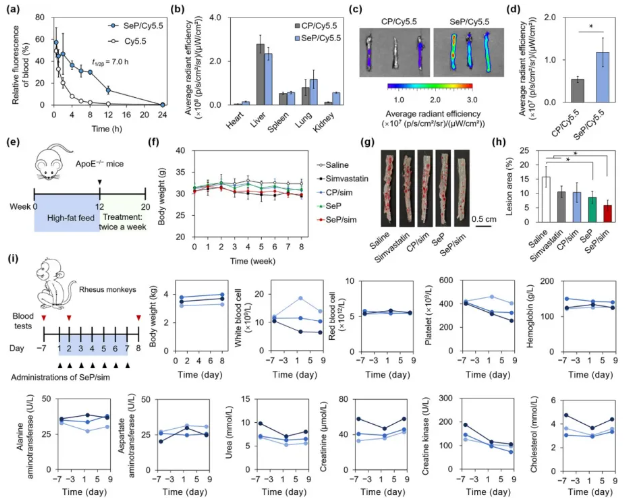
图5.硒肽纳米药物改善动脉粥样硬化的体内评价。(a)硒肽纳米颗粒在血液中的代谢情况。(b)硒肽纳米颗粒在动脉粥样硬化模型鼠(高脂饮食喂养12周的ApoE−/−小鼠)中的生物分布情况。(c)硒肽纳米颗粒在动脉粥样硬化模型鼠动脉中的富集情况。(d)主动脉荧光强度的定量分析。(e)治疗方案的示意图。(f)治疗期间小鼠的体重。(g、h)治疗后ApoE−/−小鼠主动脉的油红O染色图像以及主动脉病变面积的定量分析(n=3)。(i)硒肽纳米药物在恒河猴的体内生物安全性评估。
作者简介
易宇,国家纳米科学中心副研究员,硕士生导师。主要从事生物医用高分子材料、超分子化学研究。在Adv. Mater.、ACS Nano、CCS Chem.、Nano Res.等期刊上发表论文30余篇,主持国家自然科学基金委、科技部重点研发计划子课题、以及北京市自然科学基金委项目等。担任Nano Research、Exploration、以及《中国药科大学学报》青年编委。
王浩,国家纳米科学中心研究员,博士生导师。主要从事生物医用高分子材料、化学生物学和纳米生物材料研究。现在为纳米生物效应与安全性实验室主任,科技部重点研发计划首席科学家(2023,2019),国家万人计划领军人才(2018),国家杰出青年基金获得者(2017),科技部中青年科技创新领军人才(2017),中科院创新交叉团队负责人(2017),国家自然科学基金创新群体骨干(2017),中科院百人计划结题优秀(2016),中科院百人计划获得者(2012)。2015年提出“活体自组装”理念设计和制备生物活性材料并阐明了“Assembly/Aggregation Induced Retention (AIR)”新机制,为新型载体材料和药物的发展提出新思路。截止目前为止发表论文200余篇,包括Sci. Adv.、Nat. Commun.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Adv. Mater.、ACS Nano等,出版专著“In vivo self-assembly nanotechnology for biomedical applications”(Springer)。
课题组主页:http://www.nanoctr.cn/wanghao/
文章信息

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号