NanoRes.│长春应化所汤朝晖刘芷麟:乏氧激活的6-重氮-5-氧代-L-正亮氨酸(DON)前药纳米颗粒协同增强超声抗肿瘤效果
本篇文章版权为郑梦飞所有,未经授权禁止转载。

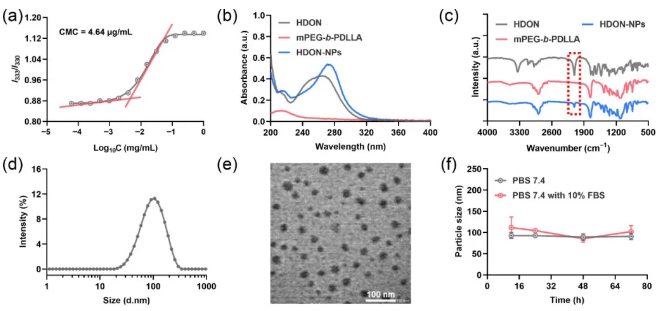
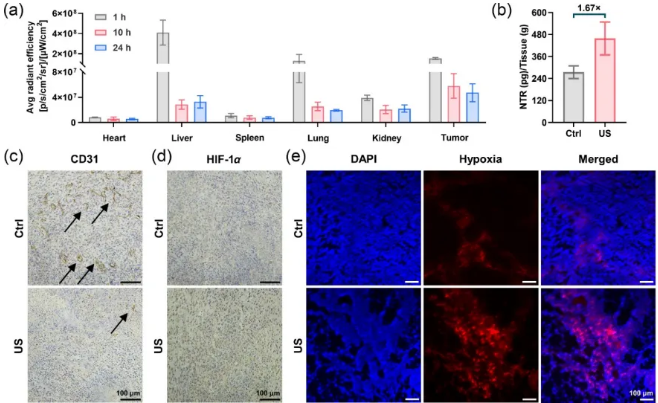
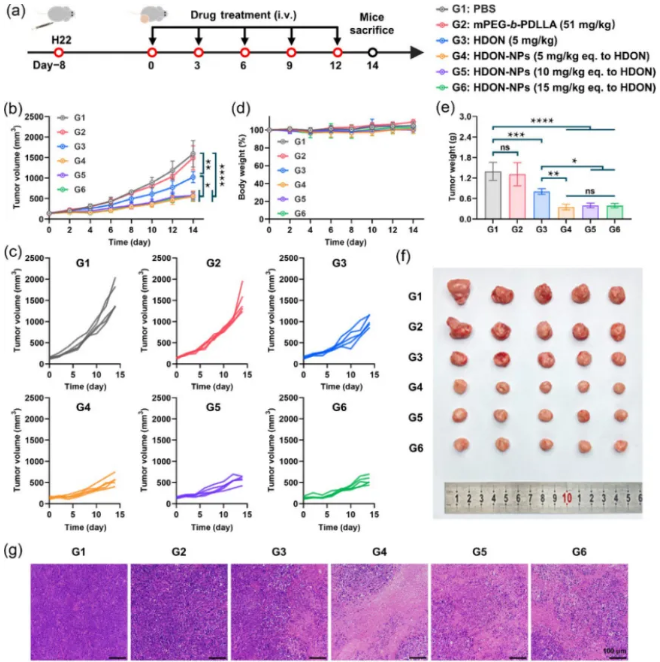
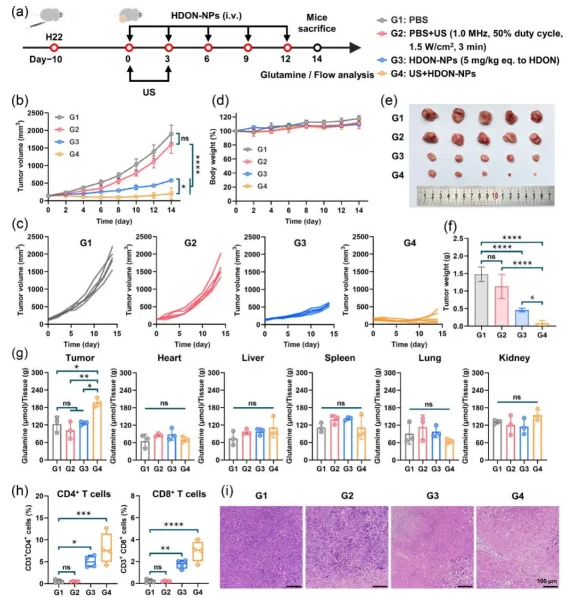
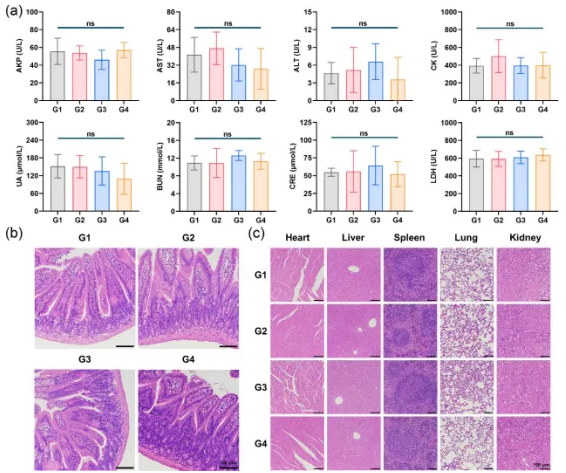
背景介绍 超声治疗是一种非侵入性技术,且具有时空性选择性,被广泛使用在临床癌症治疗中。超声因其良好的穿透性,能有效到达病变部位并治疗深部肿瘤。例如,临床中使用高强度聚焦超声(HIFU),通过将超声波聚焦在病变部位,直接杀死肿瘤细胞,从而最大限度地减少对正常组织的损伤。然而,超声单独治疗很难实现满意的抗肿瘤效果。同时,超声治疗会破坏肿瘤组织中的血管并加剧肿瘤的乏氧程度。临床试验表明,肿瘤缺氧常是患者预后和治疗不良的主要原因。然而,实体瘤的缺氧程度远高于正常组织。这为缺氧激活前药(HAPs)提供了一个新的治疗靶点。最近研究表明,肿瘤组织乏氧会导致肿瘤细胞对谷氨酰胺的摄取增加,阻断肿瘤细胞的谷氨酰胺摄取能有效抑制肿瘤的生长。因此,本研究制备了乏氧激活的谷氨酰胺拮抗剂前药纳米粒子,将超声引起的乏氧缺点转变为药物选择性激活的靶点,选择性阻断肿瘤的谷氨酰胺代谢,并协同增强超声抗肿瘤效果。 成果简介 本研究首先利用聚乳酸(mPEG-b-PDLLA)担载了我们团队之前合成的乏氧激活6-重氮-5-氧代-L-正亮氨酸前药(HDON),成功制备了HDON纳米粒子(HDON-NPs)。HDON是一种乏氧激活的谷氨酰胺拮抗剂前药,可以在乏氧的肿瘤环境中被硝基还原酶还原成DON,阻断肿瘤细胞的谷氨酰胺代谢,并激活抗肿瘤免疫反应。接着,探究了超声(US)对肿瘤组织的影响。实验表明超声可以破坏肿瘤组织的血管,并增加肿瘤组织的乏氧程度,提升肿瘤组织中硝基还原酶的表达,这有助于HDON在肿瘤组织中的还原。动物实验表明,US联合HDON-NPs取得了显著的肿瘤抑制效果,其肿瘤抑制率达90.2% ± 6.4%,具有协同效应,并且肿瘤抑制率是US单独治疗的5.93倍,未对小鼠造成明显的毒副作用。 图文导读 机理图US联合HDON-NPs治疗示意图 图1 HDON-NPs的制备表征 图2 HDON-NPs的组织分布以及US提升肿瘤组织乏氧程度 图3 HDON-NPs在小鼠H22肿瘤模型上的抗肿瘤评价 图4 US联合HDON-NPs在小鼠H22肿瘤模型上的抗肿瘤评价 图5 US联合HDON-NPs治疗后血液生化指标分析以及小肠和主要器官H&E切片分析 作者简介 郑梦飞(第一作者):中国科学院长春应用化学研究所博士生,主要研究领域为高分子纳米前药的制备与评价、肿瘤代谢阻断疗法。 刘芷麟(通讯作者):中国科学院长春应用化学研究所副研究员,入选第七批吉林省青年科技人才托举工程,主持国家自然科学基金青年项目、吉林省自然科学基金面上项目等。以第一/通讯作者在Adv Mater、ACS Nano、Adv Drug Deliver Rev、Aggregate、Biomaterials、CCS Chem、Chem Eng J、J Control Release、Nano Today等SCI期刊发表文章十余篇,任J Bionic Eng、J Neurorestoratology等期刊青年编委。 汤朝晖(通讯作者):中国科学院长春应用化学研究所研究员,国家杰出青年科学基金获得者,入选中国科学院青年创新促进会“优秀会员”。主持和参与了多项国家自然科学基金委重点和面上项目、科技部国家重大新药创制项目,研究方向为有机高分子生物医用材料,在Adv Mater、ACS Nano、Biomaterials等期刊发表文章130余篇。申请中国发明专利40余项,其中已授权专利30余项,申请PCT专利2项,获授权美国专利1项。 课题组链接:http://biopolymer.ciac.jl.cn/ 文章信息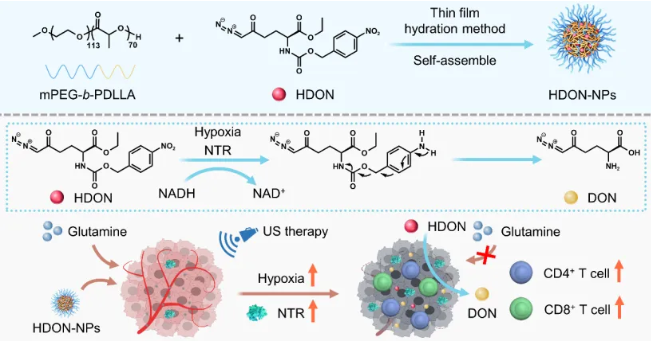

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号