单原子催化剂介导的生物正交调控N⁶-甲基腺苷甲基化促进癌症免疫治疗
作者:X-MOL
2024-03-27
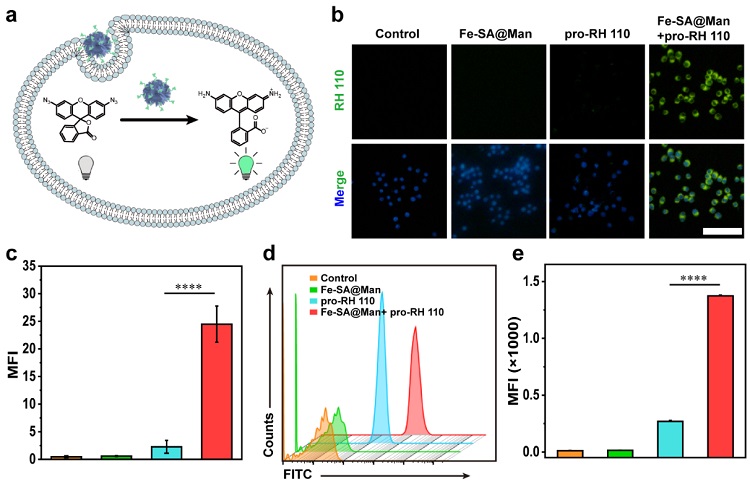
生物正交化学在不干扰正常生物过程的情况下,在细胞成像、生物分子调控和治疗应用方面取得了显著成果。尤其是肿瘤的前药激活治疗领域中,因为它可以减少药物治疗过程中的副作用,引起了相当大的关注。过渡金属催化剂 (TMC) 作为催化生物正交反应的理想候选人,一系列TMC,如Ru和Pd复合物,已被开发用于激活细胞内的蛋白质和治疗药物。然而,均相催化剂的稳定性低,在生理环境中的生物相容性差。为了克服均相催化剂的缺点,设计了生物相容的异相催化剂,实现细胞内生物正交催化抗肿瘤治疗。尽管取得了一些成就,但原子利用率低和暴露在TMC表面的活性位点较少在很大程度上限制了它们的催化活性。并且在复杂的生理条件下,TMC的反应速率仍然不能产生足够的活性物质。在改善TMC的催化和治疗方面,设计具有最大原子利用效率和良好生物相容性的高效催化平台是非常可取但是具有挑战性的。 具有原子级活性位点的单原子催化剂 (SACs) 在催化领域取得了突破性进展。作为一类全新的异相催化剂,它具有更强的催化活性和最大的金属催化剂使用效率,可以弥合均相和异相催化剂之间的差距,用于各种应用。此外,由于金属中心的活性价电子和低配位环境,SACs正在成为多功能生物催化剂,并在生理条件下对各种反应显示出优越的催化活性。基于此,中国科学院长春应用化学研究所曲晓刚 (点击查看介绍 )研究团队首次开发了硫掺杂的Fe单原子催化剂,作为一种高效的生物正交催化剂,用于细胞内催化和操纵生物过程 (图1)。由于原子尺度的活性位点和高原子利用率,Fe-SA催化剂在生物环境中即使在低浓度下也表现出优异的催化活性(图2)。
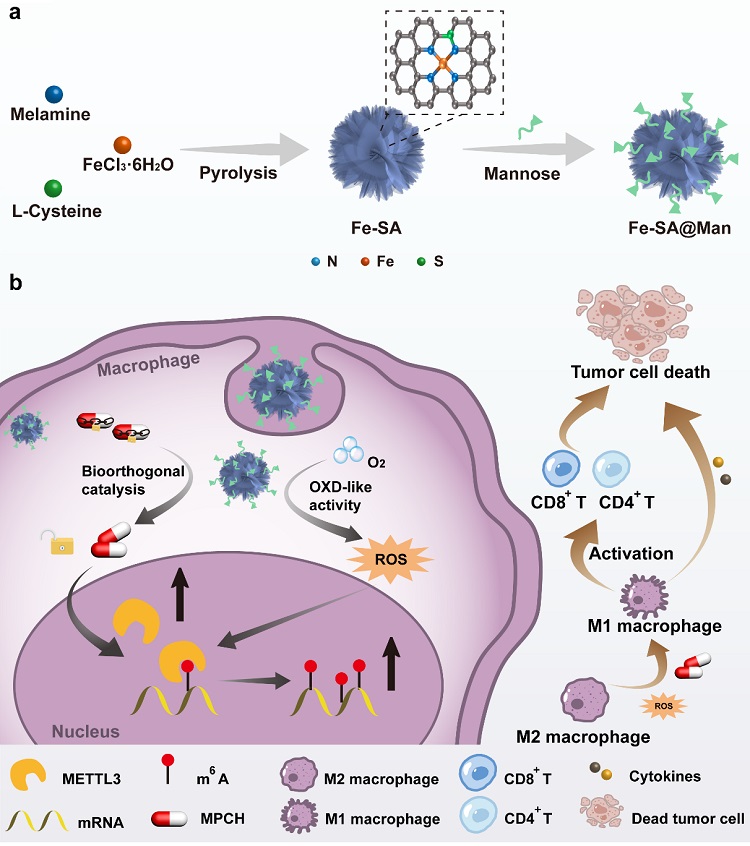
图1. 单原子催化剂介导的生物正交催化用于癌症免疫治疗的示意图总结。(a) Fe-SA@Man NCs的制备方案。(b) Fe-SA@Man NCs激活前体药物的治疗机制。
为了证明催化剂的实用性,Fe-SA@Man成功地原位调控了巨噬细胞中N 6 m 6 m 6 m 6 m 6 m 6
作为首个具有良好催化活性和生物相容性的单原子生物正交催化剂,这项工作不仅推动单原子催化剂在高效生物正交催化中的应用,而且为m 6 Journal of the American Chemical Society 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文 ):
Single-Atom Catalysts Mediated Bioorthogonal Modulation of N 6 -Methyladenosine Methylation for Boosting Cancer Immunotherapy
Mengyu Sun, Xuemeng Liu, Zhengwei Liu, Wenting Zhang, Guangming Li, Jinsong Ren*, and Xiaogang Qu* J. Am. Chem. Soc ., 2024 , DOI: 10.1021/jacs.3c12726